Post berkaitan
Apa yang MS Penghubung Silang untuk Kompleks Protein Mengajar Tentang Perubahan Formasi
2026-02-22Cross-Linking MS untuk Kompleks Protein ialah salah satu cara paling praktikal untuk "membekukan" kenalan protein sebenar di tempat dan kemudian membacanya dengan spektrometri jisim—supaya anda boleh belajar bagaimana kompleks berubah bentuk, bukan hanya rupa dalam satu syot kilat. Di Longlight Technology, kami melihat banyak pasukan bermula dengan soalan mudah: Adakah kompleks protein saya statik, atau adakah ia bertukar antara konformasi yang penting untuk fungsi? Artikel ini menerangkan, dengan cara yang mesra pemula, apakah penghubung silang kimia ditambah dengan spektrometri jisim (sering dipanggil CL-MS atau XL-MS) boleh mengajar anda tentang perubahan konformasi, dan cara menukar keputusan kepada keputusan yang boleh anda tindakkan.
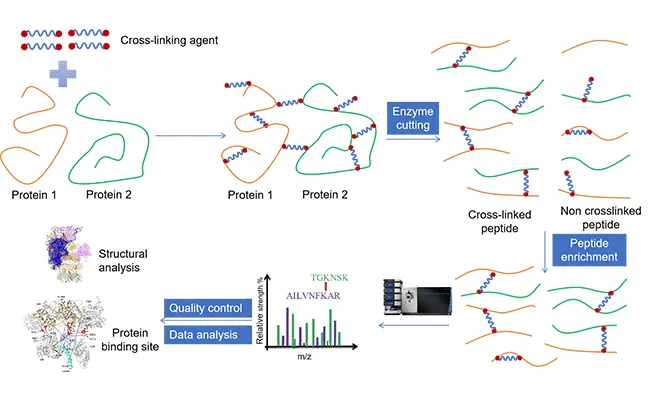
Kemajuan dalam analisis kompleks protein dengan pautan silang kimia ditambah dengan spektrometri jisim
1) Apakah MS Pautan Silang?
MS Pautan Silang (sering ditulis XL-MS atau CL-MS) ialah kaedah yang membantu anda mencari bahagian protein yang berdekatan antara satu sama lain—sama ada dalam satu protein atau antara protein dalam kompleks—dengan "menghubungkan" mereka secara kimia dan kemudian mengenal pasti pautan tersebut melalui spektrometri jisim.
Berikut ialah idea dalam bahasa Inggeris biasa:
• Tambah penghubung silang ("jambatan" kimia kecil)
Ia bertindak balas dengan asid amino tertentu dan boleh menghubungkan dua sisa secara kovalen yang berada dalam jarak terhad antara satu sama lain.
• Mencerna protein ke dalam peptida
Enzim (selalunya tripsin) memotong protein menjadi kepingan yang lebih kecil.
• Jalankan spektrometri jisim
MS mengesan peptida, termasuk pasangan peptida bersilang.
• Menganalisis pautan silang
Setiap pautan silang yang dikenal pasti menjadi kekangan jarak:
"Sisa A dan sisa B cukup rapat untuk dikaitkan dalam keadaan ini."
Untuk apa ia digunakan
• Pemetaan interaksi protein-protein (PPI): siapa yang menyentuh siapa dalam kompleks
• Pengenalpastian antara muka: kawasan mana yang membentuk permukaan sentuhan
• Perubahan formasi: bandingkan keadaan (apo vs ligan-bound, mutan vs WT) untuk melihat kenalan muncul/hilang
• Menyokong pemodelan struktur: gabungkan dengan cryo-EM/X-ray untuk mengesahkan atau memperhalusi model
Mengapa ia berharga
• Boleh menangkap interaksi yang lemah atau berumur pendek (pautan kovalen "membekukannya")
• Selalunya tiada pelabelan khas diperlukan
• Boleh menjadi pemprosesan yang agak tinggi untuk membandingkan pelbagai keadaan
2) Mengapa Perubahan Formasi Sangat Sukar To Tangkap
Banyak kompleks protein tidak duduk diam. Mereka bernafas, berputar, membuka, menutup dan menyusun semula subunit sebagai tindak balas kepada ligan, garam, pH, fosforilasi atau rakan kongsi pengikat. Kaedah struktur tradisional boleh menjadi sangat baik, tetapi mereka sering memihak kepada keadaan yang stabil. Jika kompleks itu fleksibel, dipasang dengan lemah atau berumur pendek, anda mungkin hanya melihat sebahagian daripada cerita itu.
Pautan silang membantu kerana ia boleh menghubungkan dua sisa secara kovalen yang datang dalam jarak tertentu. Dalam bahasa mudah, ia menandakan "kedua-dua kedudukan ini cukup dekat untuk disentuh" pada masa reaksi. Perbandingan pautan silang bersebelahan—bebas ligan vs terikat, garam rendah vs tinggi, jenis liar vs mutan—memberitahu anda jika kompleks dipadatkan, mengembang atau mengkonfigurasi semula.
✅ Wawasan praktikal untuk pemula: anjakan konformasi ialah anjakan ensembel. XL-MS melihat melangkaui konformasi yang paling stabil kepada spektrum keadaan dalam penyelesaian.
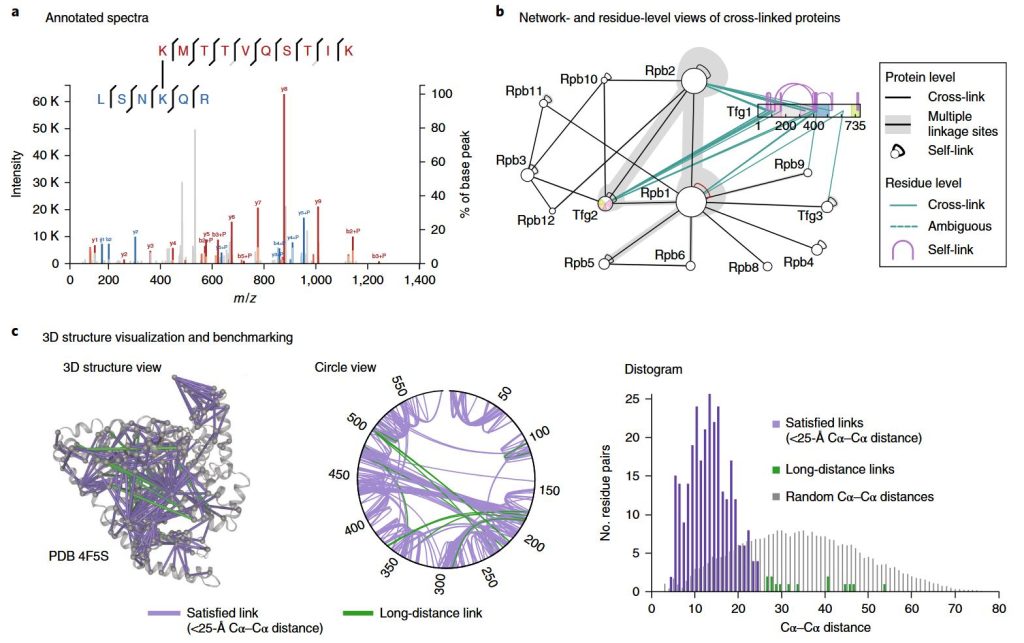
Perkhidmatan Spektrometri Jisim Crosslinking | Makmal Bio MtoZ
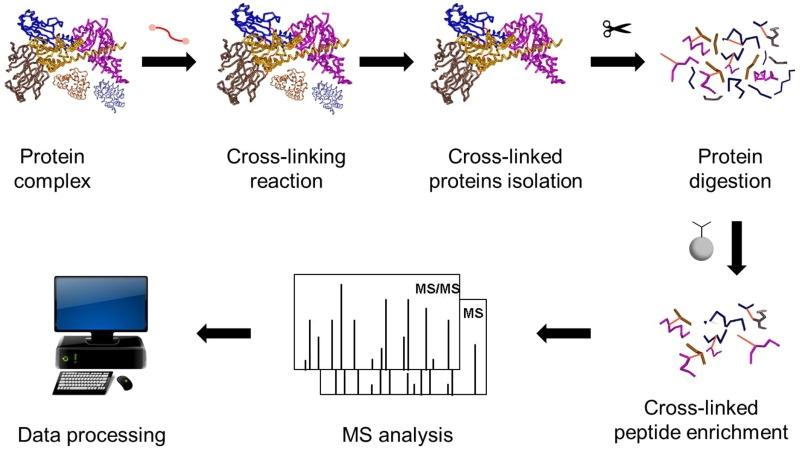
Apakah Langkah MS Penghubung Silang dalam Amalan
Penghubung silang kimia dengan MS mengukur corak kedekatan dan interaksi sisa, pendekatan standard untuk mengkaji PPI. Ejen penghubung silang bertindak balas dengan kumpulan berfungsi pada protein dan boleh menyambungkan dua atau lebih protein yang berinteraksi (atau dua kedudukan dalam satu protein). Selepas pautan silang, spektrometri jisim menganalisis peptida bersilang, membolehkan anda menggambarkan rangkaian interaksi dan mengenal pasti tapak tindakan.
Apakah maksudnya untuk perubahan konformasi?
• Jika satu set pautan silang muncul hanya selepas pengikatan ligan, ia mencadangkan kenalan baharu yang terbentuk dalam keadaan terikat.
• Jika pautan silang tertentu hilang, ini menunjukkan tapak tersebut tidak lagi dekat—mungkin kompleks dibuka atau domain bergerak.
• Jika pautan silang beralih antara subunit, ia mungkin menunjukkan penyusunan semula subunit atau laluan pemasangan yang berbeza.
✅ Apa yang anda perolehi daripada kaedah ini (dan mengapa ia penting):
• Tiada pelabelan kimia khas diperlukan → anda boleh mengekalkan protein anda dekat dengan bentuk asalnya dan mengurangkan overhed eksperimen.
• Menangkap interaksi jangka pendek/lemah → ikatan kovalen boleh mengekalkan kenalan yang sebaliknya berantakan semasa penulenan atau analisis.
• Pemprosesan tinggi dan kelajuan analisis pantas → berguna apabila anda perlu membandingkan banyak keadaan atau pembinaan dengan cekap.
• Pautan silang intraselular boleh dilakukan → untuk sesetengah projek, ini membantu anda mengkaji kompleks lebih dekat dengan konteks selular asli mereka dan bukannya hanya secara in vitro.
4) Membaca "Gerakan" Daripada Corak Pautan Silang
Pemula kadangkala mengharapkan satu pautan silang sama dengan satu jawapan. Dalam amalan, nilai datang daripada corak.
Cara yang berguna untuk berfikir ialah: pautan silang adalah kekangan jarak. Apabila kompleks berubah konformasi, jarak antara dua sisa berubah. XL-MS tidak boleh sentiasa memberitahu anda sudut putaran yang tepat, tetapi ia boleh memberitahu anda sama ada kawasan mungkin bergerak lebih dekat atau lebih jauh, dan sama ada peta interaksi berubah.
Berikut ialah cerita konformasi biasa yang boleh didedahkan oleh XL-MS:
✅ Pemadatan vs Pembukaan
Jika anda melihat lebih banyak pautan silang intra-protein yang merangkumi kawasan jauh di bawah satu keadaan, protein mungkin menggunakan keadaan yang lebih padat. Jika pautan tersebut jatuh sementara yang lain meningkat, ia mungkin terbuka.
✅ Penukaran Antara Muka
Jika pautan silang antara subunit A dan B lemah, manakala pautan antara A dan C mengukuh, ia mencadangkan pemasangan berwajaran semula atau suis antara muka.
✅ Penstabilan Mengikut Ligan Atau Mutasi
Ligan yang "mengunci" konformasi sering meningkatkan kebolehulangan set pautan silang tertentu dan mengurangkan corak campuran.
Dari sudut praktikal, ini boleh membimbing langkah seterusnya: mutan mana yang hendak dibuat, domain mana yang hendak dipotong, keadaan penimbal mana yang menstabilkan kompleks, atau antara muka mana yang hendak disahkan dengan kaedah lain.
5) Keputusan Yang Lebih Kukuh Apabila XL-MS Digabungkan Dengan Cryo-EM Atau X-Ray
XL-MS sering digunakan bersama mikroskop krio-elektron (cryo-EM) dan pembelauan kristal sinar-X untuk penyelidikan struktur biologi. Gabungan ini amat berguna apabila perubahan konformasi adalah persoalan teras.
• Cryo-EM boleh menyediakan model struktur untuk keadaan dominan.
• XL-MS boleh mengesahkan sama ada model konsisten dengan tingkah laku penyelesaian dan boleh membenderakan keadaan alternatif yang cryo-EM mungkin kurang sampel.
• X-ray boleh menyampaikan domain resolusi tinggi, manakala XL-MS membantu meletakkan domain dalam pemasangan yang fleksibel.
✅ Aliran kerja praktikal: gunakan XL-MS terlebih dahulu untuk mengetahui sama ada kompleks anda heterogen. Jika ya, anda boleh mereka bentuk keadaan yang memperkayakan satu negeri sebelum melabur banyak dalam kerja struktur resolusi tinggi.
6) Aliran Kerja Perkhidmatan At Teknologi Cahaya Panjang
Banyak makmal mahukan cerapan MS Penghubung Silang untuk Kompleks Protein tanpa membina saluran paip penuh secara dalaman. Teknologi Longlight menyokong kedua-dua pasukan berpengalaman dan pengguna kali pertama dengan proses perkhidmatan yang jelas.
Anda boleh sama ada menghantar sampel pautan silang atau menghubungi kami untuk membangunkan pelan pautan silang dan kemudian menyerahkan sampel. Kami melengkapkan aliran kerja penuh, termasuk pencernaan enzim, pengayaan peptida, pengesanan spektrometri jisim, analisis data dan penghantaran laporan eksperimen. Pendekatan hujung ke hujung ini penting kerana tafsiran konformasi bergantung pada pengendalian yang konsisten merentas langkah.
✅ Maksudnya untuk anda sebagai pelanggan:
• Kurang ralat penyerahan antara langkah, dan lebih sedikit "tidak diketahui" apabila anda membandingkan keadaan
• Laporan yang disusun berdasarkan tafsiran yang boleh diambil tindakan, bukan sahaja pengenalan mentah
• Lelaran yang lebih pantas apabila anda perlu menguji pelbagai binaan atau keadaan rawatan
Jika projek anda yang lebih luas termasuk genomik atau pembangunan ujian huluan, Longlight juga menyediakan penyelesaian genomik canggih, instrumen makmal termaju dan reagen dan bahan habis pakai berkualiti tinggi yang direka untuk meningkatkan kecekapan dan ketepatan dalam makmal moden—menyokong aliran kerja penyelidikan daripada biologi molekul kepada analisis ketepatan.
7) CTA Praktikal: Tukar Soalan Formasi Menjadi Bukti Boleh Diuji
Perubahan konformasi bukanlah perincian sampingan. Ia sering memutuskan sama ada sasaran boleh diubat, sama ada kompleks dipasang dengan betul, dan sama ada mutasi benar-benar mengganggu. Cross-Linking MS untuk Kompleks Protein memberi anda bukti yang boleh anda bandingkan merentas keadaan, yang membantu anda berhenti meneka dan mula mereka bentuk.
✅ Jika anda merancang kajian perubahan konformasi, pertimbangkan untuk bermula dengan satu "set perbandingan":
• Apo vs terikat ligan (atau terikat perencat)
• Mutan jenis liar vs satu antara muka
• Satu penimbal penstabil vs satu penimbal tekanan (julat garam/pH)
CTA: Jika anda mahukan pelan XL-MS yang jelas dan mesra pemula yang disesuaikan dengan kompleks protein anda, hubungi Longlight Technology untuk membincangkan matlamat anda (pemetaan interaksi, pengesahan antara muka atau perbandingan konformasi). Kami boleh membantu anda memilih strategi pautan silang praktikal dan menyampaikan laporan yang boleh ditafsirkan yang menyokong eksperimen anda yang seterusnya—atau model struktur anda yang seterusnya.